江西小鼠肺纖維化模型造模方法
肺間質纖維化的形成是許多慢性肺疾病的共同結局,其病理特點是長期肺部炎癥導致肺泡持續性損傷以及細胞外基質(EcM)的反復破壞、修復和改建。博萊霉素引起的急性肺損傷(ALI)可導致成纖維細胞及肌成纖維細胞的增生,這些增生的細胞可產生大量ECM,比較終導致纖維化的形成。給予博萊霉素后小鼠表現為炎癥反應,早期為急性中性粒細胞浸潤,隨后過渡為淋巴細胞增多的慢性表現,與Izbicki等“的研究結果一致。Tarnell等的研究指出,纖維化模型BALF中中性粒細胞比血液中中性粒細胞產生更多的超氧陰離子。然而這種反應是暫時的,在明顯纖維化發生之前中性粒細胞就已恢復到正常水平,所以這些細胞可能并不直接作用于纖維化的起始。在肺纖維化模型中,免疫抑制療愈對肺纖維化的進程有一定影響。江西小鼠肺纖維化模型造模方法
肺纖維化模型為科學家們提供了一個獨特的工具,使他們能夠普遍而準確地評估不同療愈肺纖維化的方法在長期內的效果。在模型中,科學家們可以模擬疾病的自然病程和進展,從而觀察并記錄療愈方法在疾病發展的不同階段所產生的影響。這種長期模擬的能力使得科學家們能夠更真實地評估療愈方法的持久性、穩定性和安全性。通過肺纖維化模型,科學家們可以對比不同療愈方法的長期效果,篩選出那些能夠明顯延緩疾病進程、改善肺功能并減少并發癥的療愈方案。這不僅為臨床提供了更可靠的療愈選擇,也為患者帶來了更大的希望。河北靠譜的肺纖維化模型實驗外包炎癥細胞的浸潤是肺纖維化模型中的一個關鍵步驟。
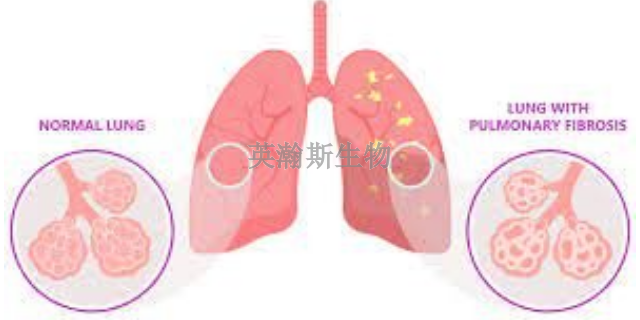
肺纖維化模型發展時間:給藥后第 7 天肺組織大多呈重度肺泡炎改變,肺泡腔及肺間質內有大量中性粒細胞浸潤,部分肺泡腔破壞或消失,肺間隔內成纖維細胞和***增生,與正常肺組織對比差別明顯;給藥后第14天,肺纖維化開始形成。巨噬細胞、中性粒細胞等炎性細胞明顯減少,成纖維細胞增多,肺泡間隔明顯增厚,有膠原沉積。給藥后第28天,多數小鼠發生彌漫性肺間質纖維化,肺間質被膠原纖維和成纖維細胞替代,肺泡壁破壞,肺大泡形成,但仍可見炎性細胞浸潤。
博萊霉素誘導的肺纖維化動物模型是廣泛應用于肺纖維化研究的模型之一,目前世界上普遍采用博萊霉素的大鼠雙側肺模型和小鼠雙側肺模型,建模方法多使用博萊霉素滴鼻建立,由于肺組織有多葉的生理結構,此兩種模型均有病變分布不均勻的情況,同時建模期間死亡率較高。本試驗采用博菜霉素誘導大鼠的單側肺纖維化動物模型,改變雙側模型中病變分布不均勻的現象,同時降低建模期間的動物死亡率,提高了成功率和動物存活率,該模型能真實模擬肺纖維化的病理過程,模型成功率高,穩定性好,死亡率低。在肺纖維化模型中,肺泡壁會逐漸增厚,導致肺功能下降。
肺間質纖維化主要特點之一就是肺問質膠原沉積,MMPs及其抑制因子在這一過程中發揮重要作用。肺泡上皮基底膜是一種特殊的ECM形式,Ⅳ型膠原是其重要組成成分。而MMP一2和MMP一9作用底物主要是Ⅳ型膠原,它們在肺纖維化發病中的作用日益受到重視。Selman等∞研究表明,特發性肺纖維化(IPF)患者MMP一2和MMP一9的過度產生可能在破壞基底膜而使成纖維細胞侵入肺泡腔引起肺纖維化中發揮一定作用。本研究結果顯示,炎癥早期MMP一2、MMP一9及TIMP一1inRNA處于正常水平,MMPs/TIMPs比例仍維持相對平衡狀態,可能是炎癥早期未出現ECM積聚之故。肺纖維化模型可以模擬肺纖維化患者的呼吸功能障礙。江西小鼠肺纖維化模型造模方法
在肺纖維化模型中,肺纖維化的發展與氧化應激和抗氧化防御系統的失衡有關。江西小鼠肺纖維化模型造模方法
肺纖維化的誤診很常見。因為盡管肺纖維化總體上并不罕見,但每種類型的肺纖維化卻均不多見,而對患者的評估需要依賴多學科的方法,因而十分復雜。疾病相關的術語已經形成了統一的標準,但在實際應用中依舊存在困難。**之間也可能對特定病例的分類持不同意見。作為一種限制性肺病,肺纖維化在肺活量測定中FEV1(第1秒用力呼氣量)和FVC(用力肺活量)均降低,因此FEV1/FVC比值正常甚至增加。這與該比值下降的阻塞性肺病形成了對比。在限制性肺病中,殘氣量和總肺活量通常都會降低。江西小鼠肺纖維化模型造模方法
- 動物阿爾茲海默癥(AD)模型建立 2025-12-24
- 山西小鼠肺纖維化模型動物實驗外包 2025-12-24
- 浙江靠譜的eae模型有哪家 2025-12-23
- 湖北專業的eae模型 2025-12-23
- 新疆靠譜的eae模型有哪些 2025-12-23
- 青海推薦的eae模型有哪些 2025-12-23
- 黑龍江靠譜的eae模型有哪家 2025-12-23
- 黑龍江eae模型是哪家 2025-12-23
- 江蘇靠譜的eae模型造模方法 2025-12-23
- eae模型造模方法 2025-12-23
- 術中顱神經監測術中神經監護跟臺 2025-12-24
- 鹽城國產遠程醫療設備監控主題 2025-12-24
- 介紹環境監測儀器產品 2025-12-24
- 陜西進口成型片廠家 2025-12-24
- 楊浦區聚醚醚酮成本價 2025-12-24
- 河北中鼻拭子供應商 2025-12-24
- 南京需求醫用激光光纖方案 2025-12-24
- 臺州醫用壓縮式霧化器口碑推薦 2025-12-24
- 提供切片功效 2025-12-24
- 專業足底壓力臺車 2025-12-24