青海eae模型動物實驗外包
EAE模型是自身免疫性腦脊髓炎(Experimental Autoimmune Encephalomyelitis)的動物模型,它是多發性硬化癥(MS)的常用研究工具。這個模型通過引起小鼠或大鼠免疫系統攻擊其自身神經組織而導致神經損傷和癥狀,從而研究MS的病理生理學、免疫學和***方法。模型的建立需要給實驗動物注射特定蛋白結構,如脊髓蛋白、腦蛋白等,以激發其免疫系統并模擬MS的癥狀。該模型的應用范圍普遍,包括探究疾病***藥物的有效性、研究免疫系統攻擊神經組織的機制等。膠原纖維酸蛋白(GFAP)也參與EAE模型的誘發。青海eae模型動物實驗外包
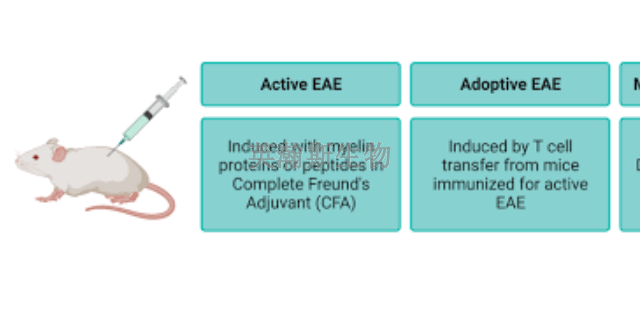
通過對EAE動物模型的基因表達分析,科學家們得以進一步深入了解多發性硬化癥(MS)的遺傳背景。這一分析過程涉及對模型動物體內基因表達水平的定量和定性研究,通過對比正常動物與EAE模型動物的基因表達差異,科學家們能夠識別出與MS發病相關的關鍵基因和基因網絡。這些基因可能涉及免疫調節、神經保護或修復等多個方面,它們的異常表達可能與MS的發病風險、疾病進程以及療愈效果密切相關。因此,對EAE動物模型進行基因表達分析不僅有助于揭示MS的遺傳機制,還為開發針對特定基因靶點的療愈方法提供了新的思路和方向。這一研究領域的進展將有助于我們更深入地認識MS這一復雜疾病,為未來的療愈和預防策略提供有力支持。湖南大鼠eae模型實驗外包EAE模型組小鼠脊髓中均出現髓鞘結構松散,密度降低等髓鞘脫失情況。
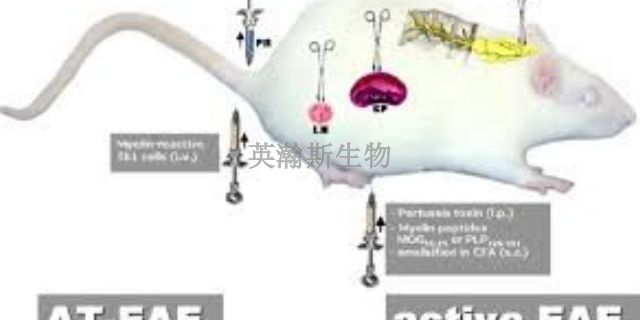
自噬在EAE模型中的研究鮮有報道,本實驗提出在EAE早期,即存在著自噬水平的降低,并貫穿疾病全程。進一步抑制自噬水平,可以促使疾病早期小膠質細胞***,增高病程中IL-1β的表達水平及炎細胞浸潤情況,加重神經功能缺損,所以EAE自噬水平的降低是導致疾病炎癥反應發***展的可能原因。這為***MS提供了新的臨床思路和***策略。但本實驗尚不能明確自噬降低的原因,有待進一步的研究。HE染色結果顯示免疫后16 d及30 d EAE+3-MA組小鼠炎細胞浸潤情況較同時間點EAE模型組加重
MOG,英文全名Myelinoligodendrocyteglycoprotein,中文名髓鞘少突膠質細胞糖蛋白,髓鞘的一種微量成分,屬于免疫球蛋白超家族成員之一。t也是特定表達于***系統(CNS)的自身抗原,誘導多發性硬化癥的原發性脫鞘特征。MOG(35-55)是髓鞘少突膠質細胞糖蛋白的免疫優勢表位,能夠誘導強烈的T細胞和B細胞應激反應,具高度致腦炎性,能夠誘導嚙齒類動物的實驗性白身免疫性腦脊髓炎(EAE)模型。EAE是**普遍的MS動物模型,具有MS許多的臨床和病理生理學特征。單次注射MOG(35-55)能夠產生一種復發-緩解型神經性疾病,表現出大量斑塊狀脫髓鞘病癥。1-甲基-4-苯基-1,.2,3,6-四氫吡啶(MPTP)誘導的多巴胺神經元損傷模型,免疫接種MOG(35-55)能抑制該神經元的白發再生功能。。EAE是一系列免疫病理和神經病理機制交叉作用引發的綜合性狀況。
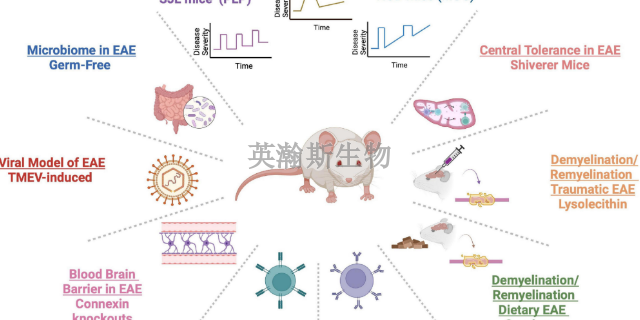
EAE動物模型的建立和應用為多發性硬化癥(MS)的研究領域注入了新的活力,提供了豐富的實驗數據和理論基礎。通過精心設計和構建EAE動物模型,科學家們能夠模擬MS在人體內的病理過程,從而深入探究疾病的發病機制、病理變化以及療愈反應。這一模型的應用不僅為科學家們提供了大量可靠的實驗數據,還幫助他們揭示了MS發病過程中的關鍵環節和分子機制。這些數據和理論基礎為MS的深入研究奠定了堅實的基礎,也為開發新的療愈方法和藥物提供了重要的參考依據。因此,EAE動物模型的建立和應用對于推動MS的研究進展具有不可替代的作用,為未來的科學研究和臨床實踐提供了新的方向和思路。小鼠、大鼠、豚鼠、家兔、羊、犬、猴等均可成功誘發EAE,在選擇動物時需要尋找EAE模型的敏感動物。湖北推薦的eae模型實驗外包
EAE小鼠模型可以反映MS的很多臨床特征。青海eae模型動物實驗外包
科學家們可以通過精細調控EAE動物模型的免疫反應,深入研究免疫療法在多發性硬化癥(MS)療愈中的潛在應用。在EAE動物模型中,科學家們可以模擬MS患者體內免疫系統的異常反應,通過調控免疫細胞的活性、數量和功能,觀察其對疾病進程的影響。這一過程不僅有助于揭示MS發病過程中免疫系統的關鍵作用,還能為開發新的免疫療法提供重要的實驗依據。通過調控EAE動物模型的免疫反應,科學家們可以測試不同免疫療法的效果,評估其對MS的療愈效果以及可能產生的副作用,從而為MS的臨床療愈提供更加安全和有效的方案。因此,調控EAE動物模型的免疫反應是研究免疫療法在MS療愈中應用的重要手段,對于推動MS的療愈進展具有重要意義。青海eae模型動物實驗外包
- 動物阿爾茲海默癥(AD)模型建立 2025-12-24
- 山西小鼠肺纖維化模型動物實驗外包 2025-12-24
- 股骨頭壞死模型構建 2025-12-24
- 浙江靠譜的eae模型有哪家 2025-12-23
- 湖北專業的eae模型 2025-12-23
- 新疆靠譜的eae模型有哪些 2025-12-23
- 青海推薦的eae模型有哪些 2025-12-23
- 黑龍江靠譜的eae模型有哪家 2025-12-23
- 黑龍江eae模型是哪家 2025-12-23
- 江蘇靠譜的eae模型造模方法 2025-12-23
- 福建人工低價定制義眼多少錢 2025-12-24
- 浦東新區國內健身器材批發 2025-12-24
- 性價比高的培養基的保質期 2025-12-24
- 陽江端粒長度基因檢測企業 2025-12-24
- 安徽口腔成型片 2025-12-24
- 重慶美容院拓客工具哪里有賣的 2025-12-24
- 重慶美容院拓客工具代理價格 2025-12-24
- 鹽田區好的體外診斷試劑市價 2025-12-24
- 無錫是什么人工智能輔助診斷設備主題 2025-12-24
- 西藏啟達醫用壓縮式霧化器專業生產廠家 2025-12-24