血液制品熱原檢測流程
來源:
發布時間:2025-11-07
MAT 法熱原檢測標曲采用非倍比稀釋,而非 1-0.5-0.25 的倍比稀釋,主要優勢在于提升標曲準確性與適用性,避免稀釋誤差影響。一是可密集覆蓋關鍵濃度區間:熱原檢測的重點關注區為低濃度拐點(如 0.0125-0.1EU/mL)與高濃度平臺區(如 0.5-1EU/mL),非倍比稀釋可在這些區間設置更多濃度點(如 0.0125、0.025、0.05、0.1、0.25、0.5、1EU/mL),提升曲線擬合精度,而倍比稀釋低濃度點少,易導致低濃度熱原定量不準。二是降低稀釋誤差累積:倍比稀釋需連續稀釋(如 1EU/mL→0.5EU/mL→0.25EU/mL),每一步誤差會累積,導致低濃度點實際濃度偏離理論值;非倍比稀釋通過單獨配制每個濃度點(如直接用標準品配制 0.025EU/mL),避免誤差累積,提升標曲可靠性。三是適配不同樣品濃度:非倍比稀釋可根據樣品預期濃度調整標曲范圍,如樣品預期濃度 0.05EU/mL,可增加 0.025、0.05、0.1EU/mL 點,確保樣品濃度落在標曲線性區,而倍比稀釋范圍固定,靈活性差。這些優勢使非倍比稀釋成為 MAT 法標曲配制的優先選擇方式。
基于人體免疫機制的 MAT 熱原檢測,為熱原檢測提供了新的可靠途徑。血液制品熱原檢測流程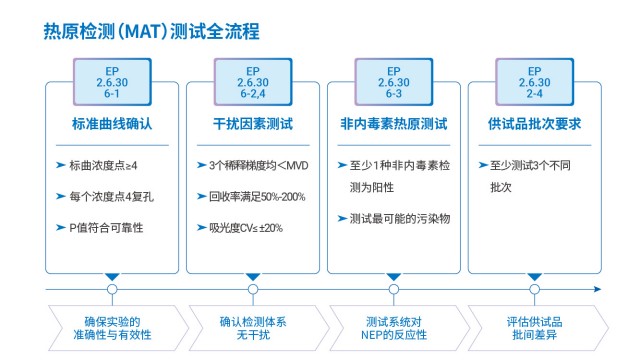
熱原檢測技術自 20 世紀初問世以來,經歷了 “動物試驗→體外生化檢測→細胞生物學檢測” 的三次關鍵變革,每一次變革均推動檢測效率、準確性與全面性的提升。20 世紀初至中期,熱原檢測方法只有家兔熱原試驗,通過觀察家兔體溫變化篩查熱原,雖實現了廣譜檢測,但存在動物成本高、操作繁瑣、靈敏度低、種屬差異大等局限,難以滿足制藥行業快速發展需求。20 世紀 60 年代,鱟試驗法(LAL 法)的發明開啟了熱原檢測的 “體外生化時代”,利用鱟血變形細胞裂解物的凝血級聯反應檢測細菌內毒素,靈敏度提升至 ng 級,檢測時間縮短至 1-2 小時,迅速成為制藥行業常規質控方法;但該方法依賴鱟資源,易受 β- 葡聚糖干擾,且只能檢測內毒素,無法覆蓋非內毒素熱原。21 世紀以來,重組技術與細胞生物學技術的發展推動熱原檢測進入 “全熱原管控時代”:重組級聯試劑(rCR)與重組 C 因子試劑(rFC)通過基因工程技術制備,擺脫對鱟資源的依賴,消除葡聚糖干擾,實現標準化生產;單核細胞活化反應測定(MAT)利用人源單核細胞檢測全類型熱原,填補非內毒素熱原檢測空白,且結果更貼近人體實際反應。
合規性熱原檢測MAT法熱原檢測技術百年演進,關鍵驅動力是靈敏度、速度與動物福利的平衡。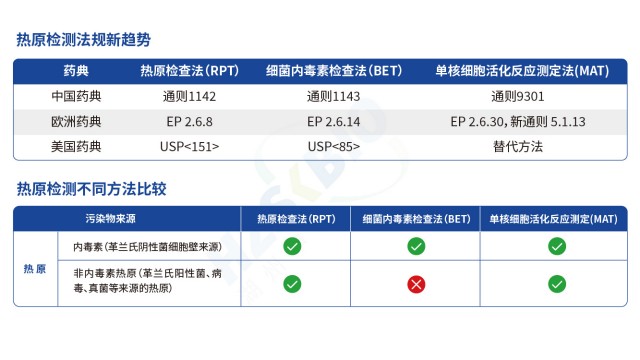
MAT法熱原檢測中,ELISA 加終止液后的讀數時間需嚴格控制,以保障 IL-6 檢測信號穩定。湖州申科生物MAT試劑盒說明書明確要求,終止液添加后需在 10 分鐘內完成讀數,且需避光操作 —— 原因在于,終止液(如硫酸)會終止 TMB 顯色反應,但生成的黃色產物在光照下易降解,超過 10 分鐘后 OD 值會下降,導致 IL-6 檢測值偏低。讀數前需進行 30 秒震蕩混勻,確保孔內液體濃度均勻,避免因局部濃度差異導致復孔 OD 值波動。酶標儀波長需設置為 450nm,若儀器含 600nm 參考波長,可同時檢測 600nm 波長以扣除背景干擾(如細胞碎片導致的光散射),提升檢測準確性。需注意的是,讀數時不可覆蓋封板膜或蓋子,避免膜上凝結的水蒸氣滴入孔中,導致 OD 值異常升高。若因儀器故障無法及時讀數,需將微孔板密封后置于 4℃避光保存,并在 30 分鐘內完成讀數,同時在記錄中注明延遲原因,評估延遲對結果的影響(如延遲 20 分鐘,OD 值可能下降 15%,需校正后使用)。
單核細胞活化反應測定(MAT)是近年來熱原檢測領域的突破性技術,其原理基于人體免疫系統對熱原的天然應答機制:人源單核細胞(如 THP-1 細胞系或新鮮人全血單核細胞)在熱原刺激下,會活化胞內炎癥信號通路,釋放 IL-6、TNF-α 等促炎細胞因子,通過 ELISA 檢測細胞因子的濃度,即可間接反映樣品中熱原的總量與活性。與傳統檢測方法相比,MAT 法具備三大不可替代的優勢:一是廣譜性,可同時檢測細菌內毒素、病毒、真菌毒素、支原體等所有類型熱原,填補了鱟試驗法只能檢測內毒素的 “非內毒素熱原盲區”,尤其適用于疫苗、基因治療產品等易受多種熱原污染的高風險產品;二是人源相關性,采用與人體同源的細胞模型,檢測結果更貼近臨床實際熱原反應,避免家兔試驗中動物種屬差異導致的誤判;三是高靈敏度,對細菌內毒素的檢測限可達 0.0125EU/mL,對非內毒素熱原(如酵母多糖、腺病毒)的檢測限低至 ng/pg 級,滿足低限值產品的質控需求。
保持細胞活性穩定,是實現準確熱原檢測的基礎條件。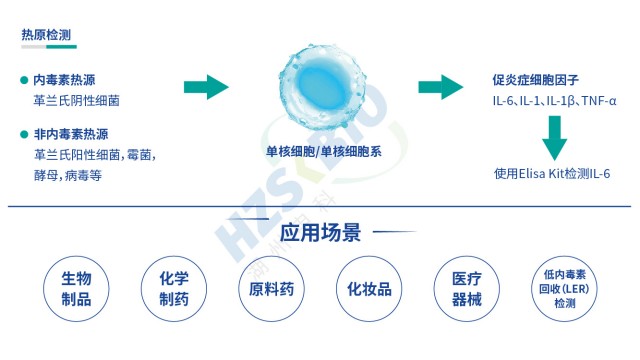
MAT法熱原檢測中,樣品與細胞共培養時長需嚴格控制,以保障炎癥因子分泌量穩定。說明書要求共培養 24 小時,雖未明確允差,但實驗驗證顯示,±30 分鐘的允差對結果無明顯影響 —— 細胞因子(如 IL-6)分泌具有時間依賴性,24 小時左右達到分泌平臺期,半小時差異不會導致分泌量大幅波動。若實驗室對結果穩定性要求極高(如 QC 放行檢測),建議嚴格按 24 小時操作,避免因時長差異引入誤差;若為預實驗(如樣品稀釋倍數摸索),±30 分鐘允差可接受,但需在記錄中注明實際培養時長。需注意的是,共培養時長不可超過 26 小時或短于 22 小時:過長會導致細胞活性下降(炎癥因子分泌減少),過短則未達分泌平臺期(檢測信號偏低),均可能導致熱原濃度低估。此外,培養環境需保持穩定(37℃、5% CO?),溫度波動會影響細胞代謝,間接導致共培養時長的實際效果偏離,因此需定期校準培養箱溫度,確保環境條件一致。
單核細胞系傳代可控,20代以內TLR表達與炎癥因子分泌保持穩定,確保熱原響應一致性。安徽高效熱原檢測湖州申科熱原檢測試劑盒聯合了國內相關機構室間驗證,與傳統RPT法結果高度一致,符合法規要求。血液制品熱原檢測流程
單核細胞系培養的高度可控性,為熱原檢測結果的可靠性提供關鍵保障。其培養基配方(如營養成分、血清濃度)可定制,確保細胞獲取充足營養;培養環境(37℃、5% CO?、濕度≥90%)可恒定控制,維持細胞好的活性與 TLR 受體表達水平,避免因環境波動導致細胞功能異常。這種可控性還能防止細胞遺傳突變與外源污染(如支原體、病毒),確保不同批次單核細胞系的熱原響應一致性,讓熱原檢測結果批間差異小,符合 GMP 對檢測方法穩定性的要求。
血液制品熱原檢測流程
上一篇
四川生物制品熱原檢測
下一篇:
河南血液制品熱原檢測
相關新聞
- 浙江qPCR法宿主細胞殘留DNA檢測常用知識 2025-12-22
- 上海高效內毒素檢測動態顯色法鱟試劑 2025-12-22
- 上海高效內毒素檢測 2025-12-22
- 四川Vero宿主細胞殘留DNA檢測常用知識 2025-12-22
- 化學制藥內毒素檢測結果判定 2025-12-22
- 上海高效熱原檢測MAT試劑盒 2025-12-19
- PG13宿主細胞蛋白(HCP)殘留檢測常見問題分析 2025-12-19
- CHO宿主細胞蛋白(HCP)殘留檢測方法學驗證 2025-12-19
- 北京高效內毒素檢測商業化試劑盒 2025-12-19
- 北京通用型宿主細胞蛋白(HCP)殘留檢測抗體制備 2025-12-19
推薦新聞
- 國產聚甲醛哪里有賣的 2025-12-23
- 河南蛋白分離純化細分技術 2025-12-23
- 江西質量灌腸器生產企業 2025-12-23
- 蘇州聚甲醛銷售廠家 2025-12-23
- 湖北醫用植絨拭子供應商家 2025-12-23
- 廣西手術示教系統 2025-12-23
- 吉林腹腔鏡醫學影像工作站銷售價格 2025-12-23
- 吉林貨號高鹽核酸酶價格表 2025-12-23
- 覆膜支架廠家報價 2025-12-23
- 貴州傷口敷料代加工 2025-12-23